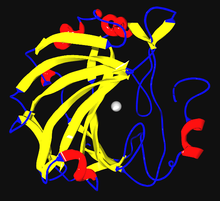
Anhydrase carbonique
| N° EC | EC |
|---|---|
| N° CAS | |
| Cofacteur(s) | Zinc |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
L'anhydrase carbonique est une enzyme qui transforme le CO2 en H2CO3 et inversement. Elle est présente chez les bactéries, les plantes et les animaux[1]. La plupart des anhydrases carboniques sont des métalloprotéines qui contiennent un atome de zinc. C'est une des enzymes les plus rapides connues[2].
Équation : H2O + CO2 H2CO3 HCO3− + H+.
Chez les vertébrés
Elle est notamment présente à la surface plasmique intracellulaire des globules rouges chez les vertébrés. Dans les reins, elle sert à libérer les protons H+.
Dans les os compacts, l'anhydrase carbonique permet de maintenir les lacunes de Howship dans un milieu acide (pH=4,5) grâce à un apport en H+
En médecine
Les inhibiteurs de l'anhydrase carbonique sont utilisés dans le traitement du glaucome ou dans l'insuffisance cardiaque.
Notes et références
- ↑ (en) Smith, K. S., Jakubzick, C., Whittam, T. S., and Ferry, J. G. (1999). Carbonic anhydraseis an ancient enzyme widespread in prokaryotes. Proc. Natl. Acad. Sci. 96, p.15184–15189
- ↑ (en) Sven Lindskog, « Structure and mechanism of carbonic anhydrase », Pharmacology & Therapeutics, vol. 74, no 1, , p. 1-20 (PMID 9336012, DOI 10.1016/S0163-7258(96)00198-2, lire en ligne)
- Portail de la biochimie
- Portail de la biologie cellulaire et moléculaire
- Portail de l’hématologie